Stopnie utlenienia pierwiastków w związkach organicznych
W dzisiejszym artykule powtórzymy wyznaczanie stopni utlenienia, na przykładach cząsteczek organicznych. Mając wiedzę z poprzednich artykułów o stopniach utlenienia, przyjrzymy się kilku związkom, a pod koniec artykułu będą zadania do rozwiązania z odpowiedziami.
Tak jak we wszystkich artykułach na stronie będziemy się posługiwać pojęciem elektroujemności w skali Pauliego.
Stopnie utlenienia w związkach organicznych
Jak wiemy z poprzednich artykułów, te same pierwiastki chemiczne mogą przyjmować różne stopnie utlenienia w tym samym związku. W chemii organicznej jest to powszechne wśród atomów węgla.
Metan, etan
Łatwo dojdziemy do wniosku, że dla węgli w metanie (CH4) i etanie (C2H6), łatwo będzie ustalić stopnie utlenienia, bazując na samym wzorze sumarycznym.
Problem zacznie się dopiero dla cząsteczek, które mają 3 więcej atomów węgla w swoich łańcuchach.
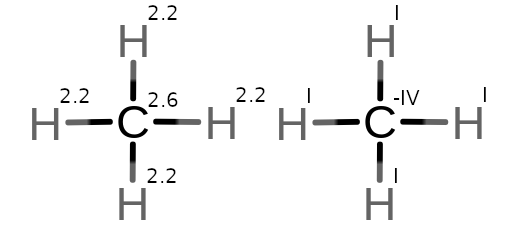
W wiązaniach H – C to węgiel przyciąga do siebie elektrony z wodoru, więc to on pozostaje bardziej elektroujemny. Węgiel w metanie będzie na IV stopniu utleniania. Łatwo też obliczyć to widząc wzór sumaryczny CH4.
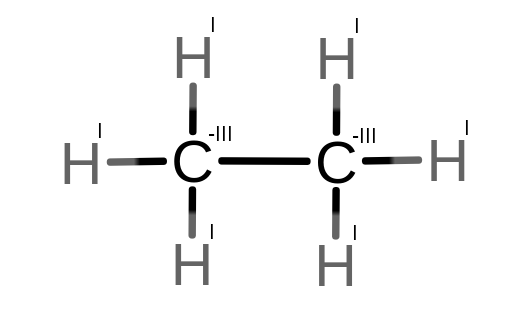
W etanie widzimy wiązanie C – C, w którym nie dochodzi do przeciągania elektronów w stronę żadnego z atomów. Z tego powodu węgle będą miały -III utlenienia.
Propan
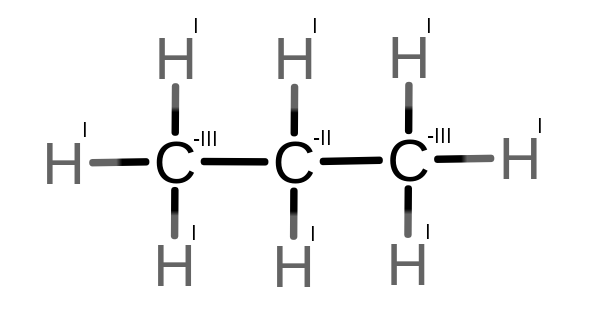
W propanie środkowy węgiel jest związany z dwoma atomami węgla, co skutkuje tym, że jest na -II stopniu utlenienia i ma wyższy stopień od pozostałych węgli. Gdybyśmy chcieli obliczyć standardowo stopień utlenienia, zakładając, że wodór będzie na I stopniu to w obliczeniach wyszłoby nam, że węgiel jest 22⁄3 stopniu utlenienia. Dlatego warto analizować stopnie utlenienia, rozpisując wzór strukturalny cząsteczki.
Azot i tlen w cząsteczkach organicznych
W metyloaminie (CH3CN2), azot jest bardziej elektroujemny od węgla i od wodoru, więc będzie on “zabierał” elektrony od atomów, z którymi tworzy wiązanie.
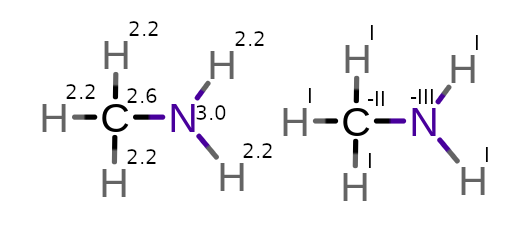
Węgiel najpierw przeciąga do siebie elektrony z trzech wodorów, z którymi ma wiązanie, a następnie azot przeciąga jeden elektron od węgla do siebie.
Azot pobiera jeszcze z wodorów po elektronie, będzie miał -III utlenienia.
W cząsteczce etanoamidu (CH3CO−NH2) od węgla bardziej elektroujemnymi atomami jest tlen i azot.
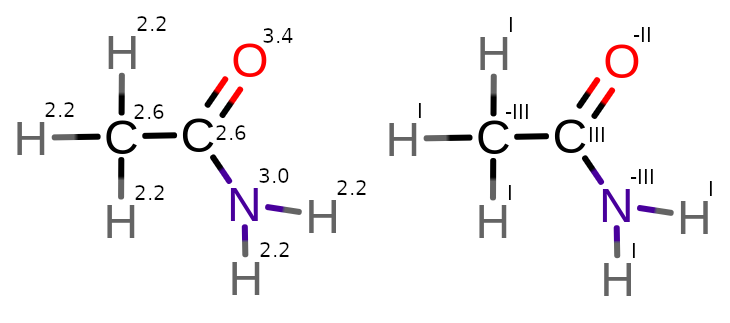
Atom węgla połączony z tlenem traci 2 elektrony i jeszcze 1 elektron na rzecz azotu. Jest związany również z drugim atomem węgla, co nie wpływa na jego bilans elektronowy. Przez taką kombinację wiązań, jeden atom węgla jest na III stopniu utlenienia a drugi na -III.
Zadania
Wypisz dla poniższych cząsteczek poprawnie ich stopnie utlenienia.
- propen
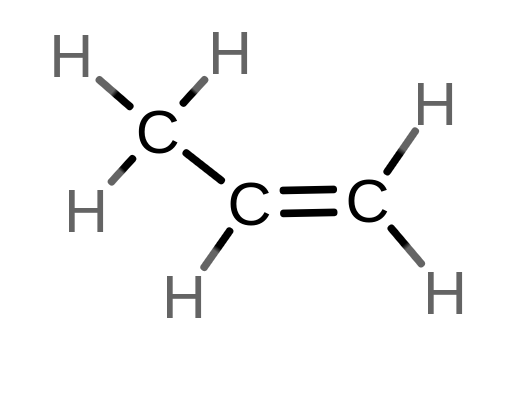
2. propyn
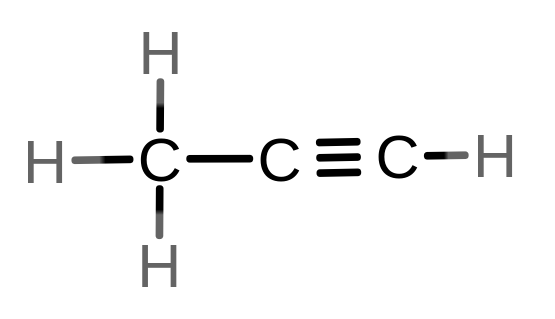
3. metanol
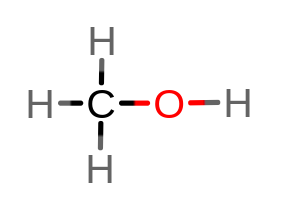
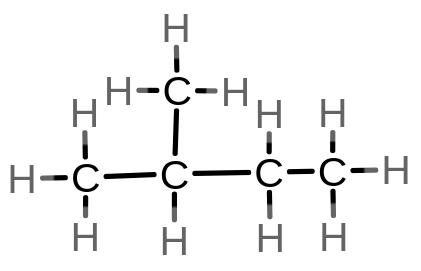
4. 2-metylobutan
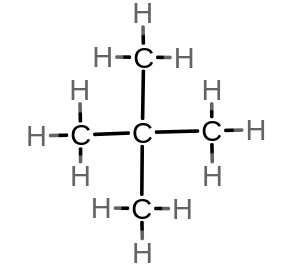
5. 2,2-dimetylopropan (neopentan)
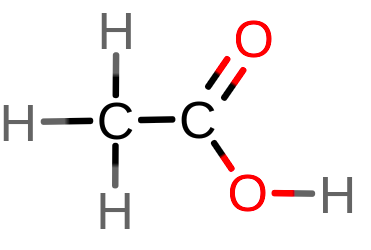
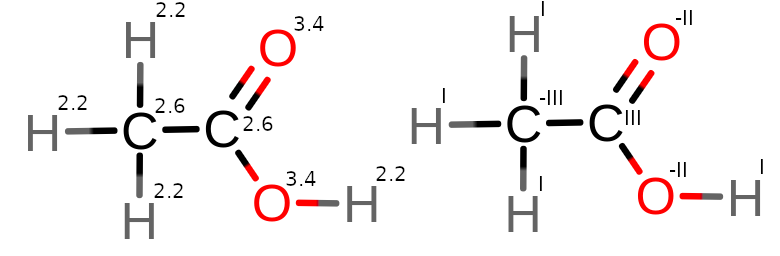
6. kwas etanowy (kwas octowy)
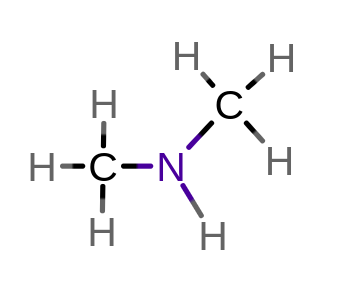
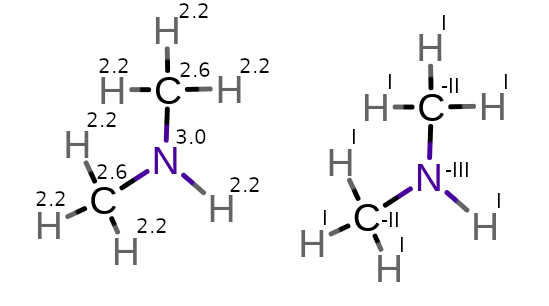
7. dimetyloamina
1.
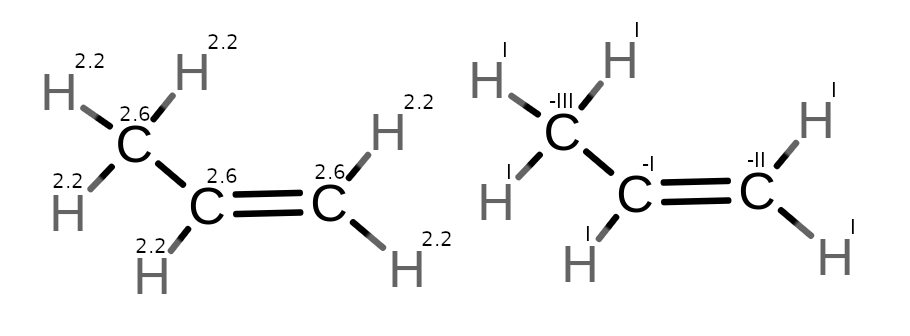
2.

3.
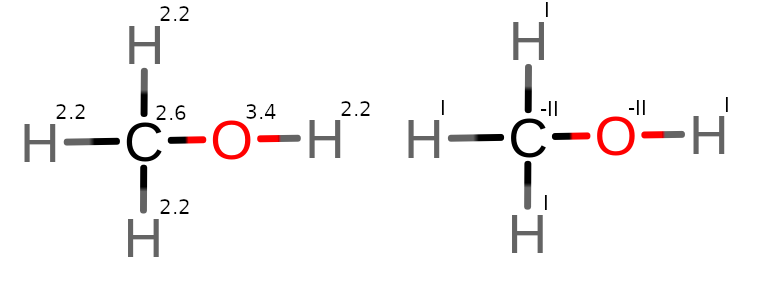
4.
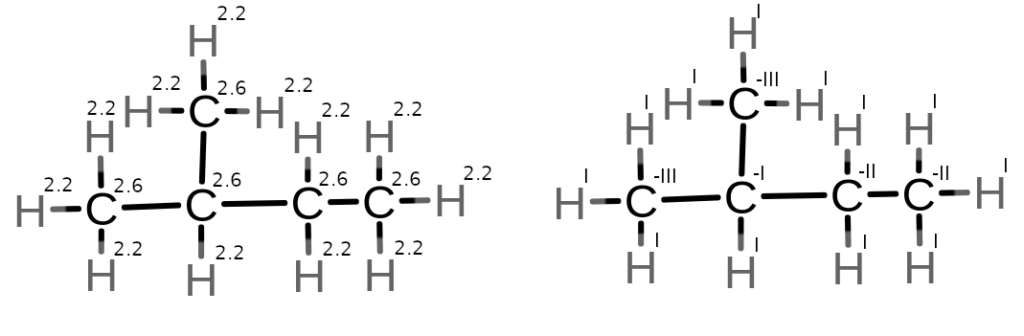
5.
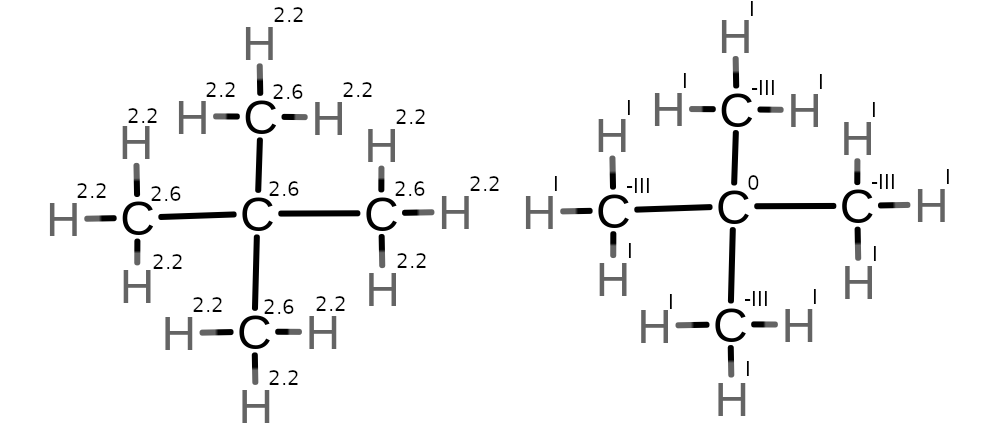
6.
7.
0 Komentarzy